可注射、光固化CAR-T水凝胶,治疗实体瘤新发现!
实体瘤是人类死亡的主要原因之一,一直是医学界面临的巨大挑战。虽然一些实体瘤患者的寿命可以通过传统的手术治疗延长,但手术切除并不适合所有病例。此外,放化疗在提高患者生存率的同时,也不可避免地伴随着副作用,治疗后肿瘤复发的现象屡见不鲜。
鉴于此,四川大学生物治疗国家重点实验室王玮研究员和门可研究员团队合作,开发了一种基于光交联甲基丙烯酰化(GelMA)水凝胶,可注射的CAR-T细胞局部递送体系(i-GMD)。GelMA水凝胶不仅可以保持良好的溶解性,而且可以通过紫外线照射形成三维结构。特殊的结构可以支持CAR-T细胞在肿瘤微环境中的存活和增殖。无需破坏性的手术操作,就可以延长CAR-T细胞在肿瘤部位的停留时间,并逐渐释放,消灭肿瘤细胞。另外,该体系可以装载各种药物,包括细胞因子、抗体、检查点抑制剂或其他药物,进一步提高抗肿瘤效率。
作者证明,基于GelMA的水凝胶可以在不影响生物功能的前提下支持重编程淋巴细胞的存活。而且,这种多功能递送系统增强了CAR-T细胞在免疫活性小鼠中的抗肿瘤作用。相关成果近期发表于《Biomaterials》。
用于CAR-T细胞治疗的i-GMD系统设计
基于GelMA水凝胶良好的生物相容性、生物降解性和机械性能,本研究选择其作为CAR-T细胞的支架。GelMA的溶胶-凝胶转变机理如下,在405 nm波长光的照射下,光引发剂LAP(苯基-2,4,6-三甲基苯甲酰基次膦酸锂)会释放自由基并引发GelMA的交联反应形成水凝胶。冻干的GelMA可以在37 °C下溶解在细胞培养基中,然后在405 nm蓝光下固化。这种原位溶胶-凝胶转换特性为CAR-T细胞提供模拟的肿瘤微环境。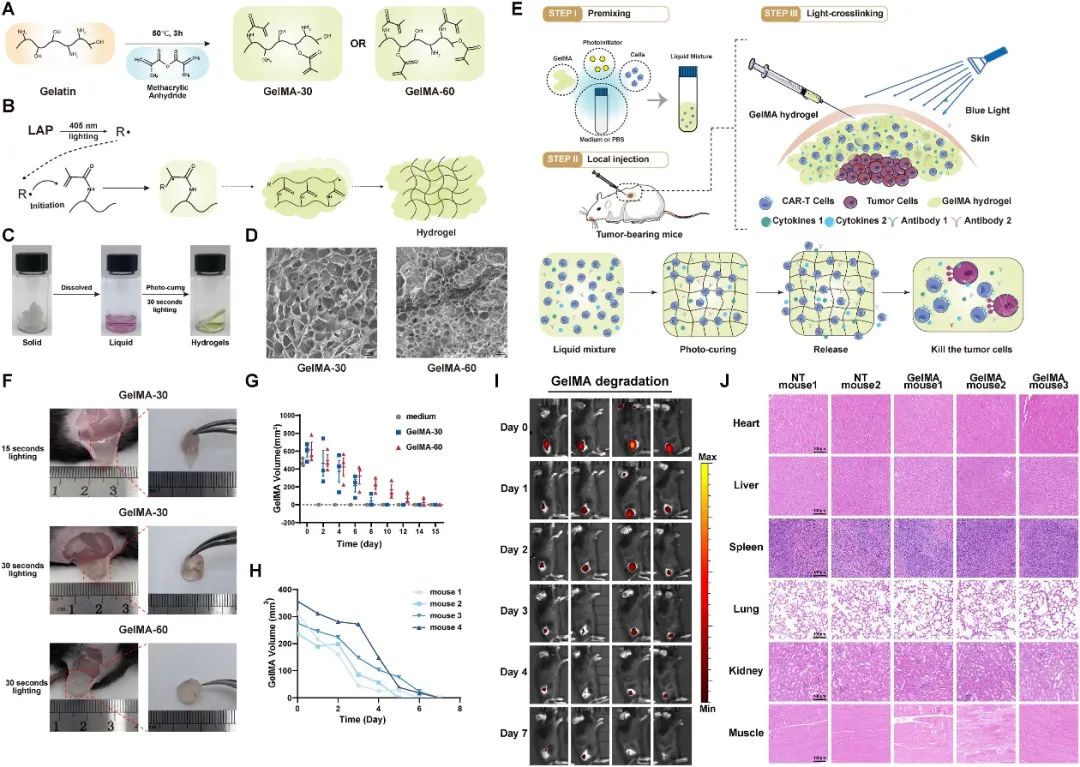
图1:基于GelMA水凝胶的免手术可注射CAR-T细胞输送系统的示意图。该水凝胶具有生物相容性和降解性。
I-GMD系统不损害CAR-T细胞的功能
CAR-T细胞的正常增殖和迁移是发挥抗肿瘤作用的必要前提之一。由于小鼠肿瘤细胞系不表达Her-2抗原,作者首先建立Her-2 + B16细胞系作为阳性靶细胞。分离原代小鼠淋巴细胞用于制备Her-2 CAR-T。为了验证培养基或GelMA中CAR-T细胞的活化,作者通过流式细胞术比较了T细胞活化标志物CD69和CD25的表达。结果表明,在没有Her-2抗原刺激的情况下,光交联水凝胶不会诱导CAR-T细胞的非特异性活化。此外,在没有抗原刺激的情况下,在GelMA中培养的CAR-T细胞也保留了低水平的衰竭标志物。表型分析表明GelMA水凝胶作为一种载体不会引发CAR-T衰竭。总体而言,递送平台中的CAR-T细胞保留了生物学功能和特性,i-GMD系统适用于储存和释放CAR-T细胞。
图2:递送系统保留了CAR-T细胞的全部功能。
I-GMD 系统在体外表现出强大的抗肿瘤功效
为了验证细胞毒性的效果,将未转导的T细胞、Mock-T、CAR-T细胞分别封装在水凝胶中,并与Her2+B16肿瘤细胞共培养。48小时后,当GelMA水凝胶装载CAR-T细胞时,B16细胞的比例降低。此外,与其他组相比,T细胞的比例也更高。相反,当未转导的T细胞或Mock-T细胞被封装到水凝胶中时,B16细胞和T细胞的百分比没有变化。与流式细胞术的结果一致,作者检测到装载有CAR-T细胞的水凝胶中分泌更多的IFN-γ和TNF-α。总的来说,这些结果表明装载CAR-T的i-GMD系统在体外显示出有效的抗肿瘤功效。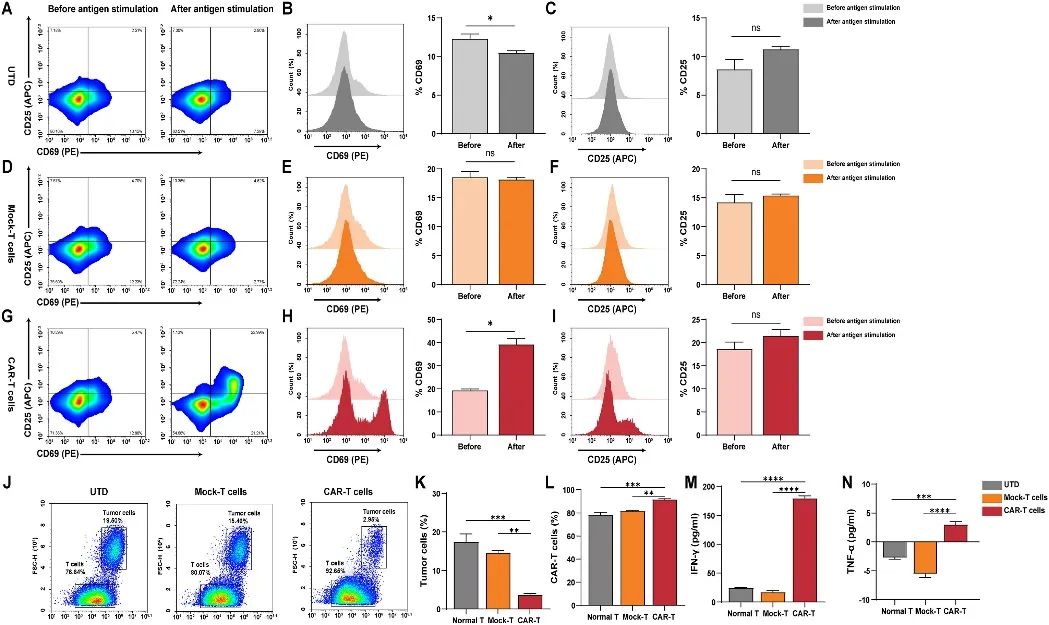
图3:I-GMD系统体外抗肿瘤效果。
I-GMD系统体内抗肿瘤机制的研究
为了验证CAR-T局部给药系统的体内抗肿瘤功效,作者通过皮下接种荧光素酶标记的 Her-2+B16细胞在免疫活性小鼠中建立了黑色素瘤模型。不同治疗组的个体和平均肿瘤体积测量结果表明,水凝胶递送的CAR-T细胞的治疗策略显示出最佳的抗肿瘤效果。此外,来自i-GMD的CAR-T细胞具有更高的活化标志物CD69和CD25的表达。所有流式细胞仪数据表明,i-GMD系统在体内可能具有更持久和有效的抗肿瘤效率。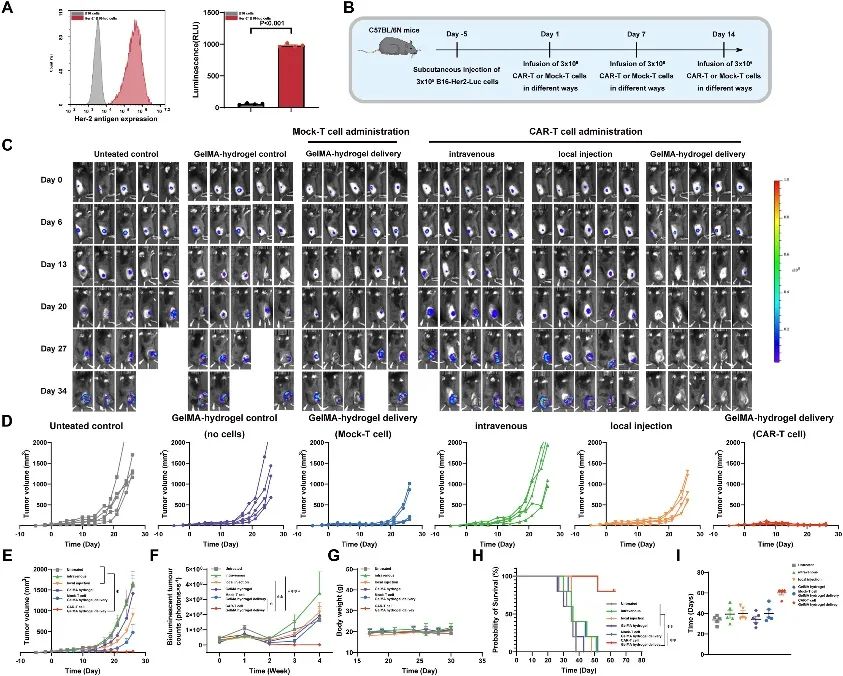
图4:I-GMD系统体外抗肿瘤效果。
总结
在这项研究中,作者设计了一种基于免手术可注射光固化水凝胶的多功能集成体系,在肿瘤部位连续提供肿瘤抗原特异性CAR-T细胞。研究结果表明,由生物相容性水凝胶递送的CAR-T细胞比静脉内或局部注射CAR-T细胞表现出更好的肿瘤根除效果。该治疗策略具有优势包括:1. 无需手术即可轻松植入。2. 可调节的物理和化学性质。3. 递送装置可以扩展多种功能。在未来,多功能递送系统在许多领域具有巨大的应用潜力,包括药物递送、伤口修复、再生医学等。
版权申明:














